Bạn đang xem bài viết Tính chất hoá học của muối là gì? Bài tập Hoá lớp 9 tại thcshuynhphuoc-np.edu.vn bạn có thể truy cập nhanh thông tin cần thiết tại phần mục lục bài viết phía dưới.
Muối là một loại hợp chất không hữu cơ mà người ta thường gặp trong cuộc sống hàng ngày. Tính chất hoá học của muối đã và đang là đề tài nghiên cứu quan trọng trong môn học Hóa học. Muối có sự tồn tại phổ biến trong các loại mì, bánh mì, nước mắm, nước uống,… và được sử dụng trong nhiều ngành công nghiệp khác nhau. Việc hiểu rõ về tính chất hoá học của muối là cần thiết để áp dụng trong các quy trình tách, tổng hợp và sử dụng của nó. Bài tập hóa lớp 9 về tính chất hoá học của muối giúp các em học sinh nắm vững kiến thức cơ bản về muối và rèn luyện kỹ năng phân tích, tổng hợp và ứng dụng kiến thức vào thực tế.
Trong đời sống, khi nói đến muối thì đó là một loại gia vị có vị mặn. Tuy nhiên, đối với hóa học, muối có nhiều loại khác nhau. Vậy tính chất hóa học của muối là gì? Cùng Chúng Tôi khám phá nhé!
Muối là gì?
Muối là gì?
Trong hóa học, muối là một khái niệm chung dùng để chỉ một hợp chất. Hợp chất của muối gồm nhiều nguyên tử kim loại liên kết với một hay nhiều gốc axit tạo thành.
Cùng Chúng Tôi tìm hiểu những thành phần và tính chất hoá học của muối kỹ hơn ngay sau đây nhé!

Thành phần hoá học của muối
Thành phần hoá học của muối có công thức hoá học gồm một hay nhiều nguyên tử kim loại (Na,Cu,Al,…) hoặc gốc amoni NH4+ kết hợp với một hay nhiều gốc axit (Cl-,SO42-,PO43-,…).
Tên muối = tên kim loại (thêm hóa trị nếu kim loại có nhiều hoá trị) + tên gốc axit.
Ví dụ:
- Na2SO4: natri sunfat.
- Fe(NO3)3: sắt (III) nitrat.
- KHCO3: kali hiđrocacbonat.
Chú ý:
- – Cl: clorua.
- =S: sunfua.
- = SO3: sunfit.
- = SO4: sunfat.
- =CO3: cacbonat.
- ≡ PO4: photphat.
Phân loại muối
Theo thành phần hoá học của muối có thể chia làm hai loại:
Muối trung hoà:
- Muối trung hoà là muối mà trong gốc axit không có nguyên tử hiđro H có thể thay thế bằng nguyên tử kim loại.
- Ví dụ: Na2SO4, Na2CO3, CaCO3.
Muối axit:
- Muối axit là muối mà trong đó gốc axit của phân tử còn nguyên tử hiđro H chưa được thay thế bằng kim loại.
- Ví dụ: NaHSO4, K2HPO4, Ba(HCO3)2,…
- Hoá trị của gốc axit bằng số nguyên tử hiđro H đã được thay thế bằng kim loại.
Chắc hẳn qua những câu hỏi trên đây bạn đã biết khái niệm và thành phần của muối hóa học. Tiếp tục cùng Chúng Tôi khám phá chi tiết tính chất hoá học của muối nhé!
Tính chất hóa học của muối
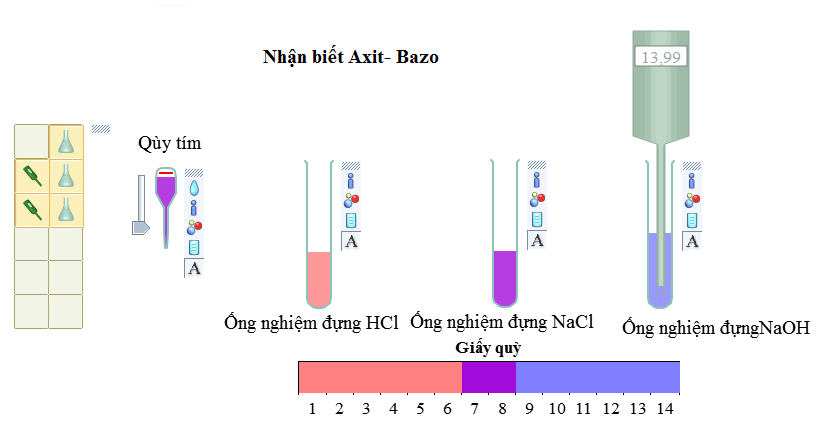
Muối làm đổi màu chất chỉ thị màu
Tính chất hoá học của muối đầu tiên của muối là làm thay đổi màu chất chỉ thị màu.
- Khi kim loại mạnh kết hợp với gốc axit yếu thì dung dịch muối đó sẽ làm đổi màu quỳ tím thành màu xanh. Ví dụ: Na2CO3, KBr, K2CO3,…
- Khi kim loại yếu kết hợp với gốc axit mạnh thì dung dịch muối đó sẽ làm đổi màu quỳ tím thành đỏ. Ví dụ: Ag2SO4,…
- Khi kim loại mạnh kết hợp với một gốc axit mạnh hoặc cả 2 có tính chất ngang nhau thì dung dịch muối đó sẽ không đổi màu quỳ tím. Ví dụ: KNO3, NaCl, CuSO3,…
Kết luận: muối có tính axit mạnh hơn làm quỳ tím hóa đỏ. Nếu tính bazơ mạnh hơn làm quỳ tím hóa xanh và quỳ tím không đổi màu khi muối đó trung tính.
Tác dụng với kim loại
Tính chất hoá học của muối tiếp theo là tác dụng với kim loại. Điều kiện: Kim loại mạnh hơn đẩy kim loại yếu hơn ra khỏi muối.
Muối tác dụng với kim loại → muối mới + kim loại mới. Như K > Na > Ca > Mg > Al > Zn > Fe > Ni > Sn > Pb > H > Cu > Hg > Ag > Pt > Au.
Ví dụ:
- Fe + CuSO4 → FeSO4 + Cu↓.
- Cu + 2AgNO3 → Cu(NO3)2 + 2Ag↓.

Phản ứng phân huỷ muối
Tính chất hoá học của muối không chỉ tác dụng với kim loại, axit. Mà bản thân muối cũng có phản ứng phân hủy riêng. Nhiều muối bị phân hủy ở nhiệt độ cao như: KClO3, KMnO4, CaCO3,…
Ví dụ:
- 2KClO3 →t0 2KCl + 3O2.
- CaCO3CaCO3 t0→ CaO + CO2.
Tác dụng với axit
Kế tiếp tính chất hoá học của muối là tác dụng với axit. Điều kiện: Axit mới yếu hơn axit phản ứng hoặc muối mới không tan trong axit mới. Tác dụng với axit → muối mới + axit mới.
Ví dụ:
- BaCl2 + H2SO4 → 2HCl + BaSO4↓.
- CaCO3 + 2HCl → CaCl2 + CO2CO2↑ + H2O.
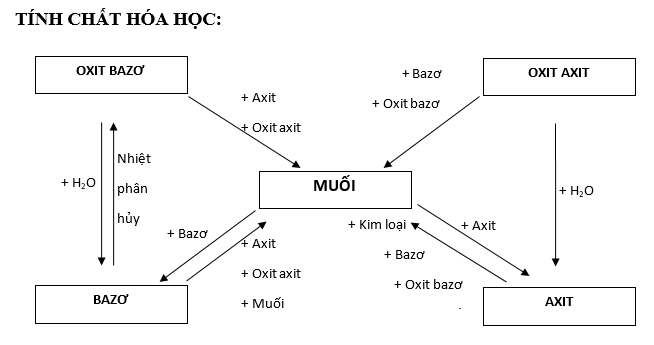
Tác dụng với dung dịch muối
Tính chất hoá học của muối đặc biệt nhất là muối có thể tác dụng với dung dịch muối tạo thành 2 muối mới.
Ví dụ:
- NaCl + AgNO3 → AgCl ↓+ NaNO3.
- Na2SO4 + BaCl2→ BaSO4↓ + 2NaCl.
Tác dụng với dung dịch bazơ
Tính chất hoá học của muối cuối cùng là tác dụng với dung dịch bazơ. Muối có thể tác dụng với dung dịch bazơ tạo thành muối mới và bazơ mới.
Ví dụ:
- Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3↓.
- NaOH + FeSO4 = Fe(OH)2 + Na2SO4.
- NaOH + FeS = Na2S + Fe(OH)2.
Bài viết liên quan:
- Tổng hợp 5 tính chất hóa học của bazơ bạn nên biết
- Tính chất hóa học của axit? 5 ứng dụng axit phổ biến nhất
- Tính chất hóa học của kim loại? 6 ứng dụng kim loại phổ biến nhất
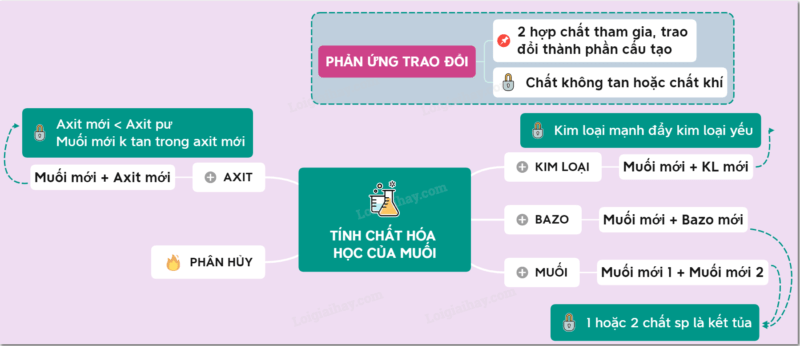
Phản ứng trao đổi dung dịch muối
Phản ứng trao đổi là gì?
Phản ứng trao đổi là phản ứng hóa học. Trong đó hai hợp chất tham gia phản ứng trao đổi với nhau để tạo ra những hợp chất mới. Trong phản ứng trao đổi, số oxi hóa của các nguyên tố trong phản ứng không thay đổi.
Ví dụ:
- NH4NO3 + BaCl2 → NH4Cl + Ba(NO3)2.
- ZnSO4 + MgCl2 + Na3PO4 → ZnCl2 + Mg3PO42 + Na2SO4.
- Na2CO3+CaCl2 →CaCO3 +NaCl.
Điều kiện xảy ra phản ứng trao đổi
Điều kiện để phản ứng trao đổi xảy ra: nếu sản phẩm được tạo thành trong quá trình trao đổi là chất khí hay chất không tan.
Ví dụ:
- K2SO4 + NaOH: Phản ứng không xảy ra.
CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2↓
Lưu ý: phản ứng trung hòa cũng thuộc loại phản ứng trao đổi luôn xảy ra.
Ví dụ:
- H2SO4 + 2NaOH → Na2SO4 + 2H2O.
Một số bài tập về tính chất hoá học của muối lớp 9
Bài 1. Trang 33 Hóa 9 bài 9. Hãy dẫn ra một dung dịch muối khi tác dụng với một dung dịch chất khác thì tạo ra:
- Chất khí.
- Chất kết tủa.
Viết các phương trình hóa học.
Hướng dẫn giải bài 1:
Dựa vào tính chất hoá học của muối, ta có những PTHH sau đây:
Tạo ra chất khí
Ví dụ muối cacbonat (CaCO3, Na2CO3, NaHCO3) hoặc dung dịch muối sunfit (Na2SO3) tác dụng với axit (HCl, H2SO4 loãng):
- CaCO3 + H2SO4 → CaSO4 + CO2 ↑ + H2O.
- Na2CO3 + 2HCl → 2NaCl + CO2 ↑ + H2O.
- Na2SO3 + H2SO4 → Na2SO4 + SO2 ↑ + H2O.
Tạo chất kết tủa
Ví dụ dung dịch muối (BaCl2, Ba(CH3COO)2, Ba(NO3)2,…) tác dụng với dung dịch H2SO4 tạo ra kết tủa BaSO4.
- BaCl2 + H2SO4 → BaSO4 ↓ + 2HCl.
- Ba(CH3COO)2 + H2SO4 → BaSO4 + 2CH3COOH.
Hoặc những dung dịch muối bari tác dụng với dung dịch muối cacbonat (Na2CO3, K2CO3) tạo ra BaCO3 kết tủa.
- Ba(NO3)2 + Na2CO3 → BaCO3 ↓ + 2NaNO3.
Bài 2. Trang 33 Hóa 9 bài 9. Có 3 lọ không nhãn, mỗi lọ đựng một dung dịch muối: CuSO4, AgNO3, NaCl. Hãy dùng những dung dịch có sẵn trong phòng thí nghiệm để nhận biết chất đựng trong mỗi lọ.
Viết các phương trình hóa học và cho biết tính chất hoá học của muối.
Hướng dẫn giải bài 2:
Dựa vào tính chất hoá học của muối, ta có những PTHH sau đây:
Dùng dung dịch NaCl tự pha chế để nhận biết dung dịch AgNO3. Xuất hiện chất kết tủa trắng AgCl.
AgNO3 + NaCl → AgCl ↓ + NaNO3 .
Dùng dung dịch NaOH trong phòng thí nghiệm để nhận biết dung dịch CuSO4 màu xanh lam.
CuSO4 + NaOH → Cu(OH)2 + Na2SO4.
Dung dịch còn lại trong lọ không nhãn là dung dịch NaCl.
Bài 3. Có những dung dịch muối sau: Mg(NO3)2, CuCl2. Vận dụng tính chất hoá học của muối cho biết muối thể tác dụng với những chất nào sau đây:
- Dung dịch NaOH.
- Dung dịch HCl.
- Dung dịch AgNO3.
Nếu có phản ứng, dựa vào tính chất hoá học của muối hãy viết các phương trình hóa học.
Hướng dẫn giải bài 3:
Dựa vào tính chất hoá học của muối, ta có những PTHH sau đây:
- Tác dụng với dung dịch NaOH là dung dịch các muối Mg(NO3)2 và CuCl2 vì sinh ra
- Mg(OH)2 kết tủa, Cu(OH)2 kết tủa.
- Mg(NO3)2 + 2NaOH → Mg(OH)2 ↓ + 2NaNO3.
- CuCl2 + 2NaOH → Cu(OH)2 ↓ + 2NaCl.
- Không muối nào tác dụng với dung dịch HCl.
- Tác dụng với dung dịch AgNO3 là dung dịch muối CuCl2 tạo AgCl kết tủa trắng. PTHH: CuCl2 + 2AgNO3 → 2AgCl ↓ + Cu(NO3)2.

Hy vọng các bạn biết được công thức hóa học của muối cùng một số bài tập về tính chất hoá học của muối lớp 9. Đừng quen share và follow bài viết để Chúng Tôi có thêm động lực chia sẻ kiến thức nữa nhé.
Tính chất hoá học của muối là các đặc điểm mà muối thể hiện trong các phản ứng hoá học. Muối là hợp chất ion có thể tạo thành từ phản ứng giữa axit và bazơ, trong đó nguyên tử hoặc nhóm nguyên tử tích điện dương trong bazơ thay thế vào ion hidro hoá trị tương ứng trong axit.
Muối thường có tính chất ổn định và dễ tan trong nước. Khi muối tan trong nước, các liên kết ion trong muối bị phá vỡ và muối phân ly thành các ion dương và ion âm. Đặc điểm này làm cho muối có khả năng dẫn điện trong dung dịch.
Một số muối có màu sắc khác nhau. Điều này được giải thích bởi khả năng của các ion trong muối hấp thụ ánh sáng trong phạm vi một số bước sóng nhất định. Ví dụ, NaCl màu trắng, CuSO4 màu xanh, FeCl3 màu vàng.
Muối cũng có khả năng tạo kết tủa khi hợp lý. Khi muối đưa vào dung dịch chứa các ion phản ứng trái ngược, các cation và anion có thể kết hợp với nhau để tạo thành kết tủa. Ví dụ, khi dung dịch NaCl được pha loãng với dung dịch AgNO3, kết tủa trắng AgCl được tạo thành.
Ngoài ra, muối cũng thể hiện tính chất oxi hóa – khử. Một số muối có khả năng oxi hóa, như KMnO4, có thể tác động lên các chất khác và tăng hoá trị của một số nguyên tố. Trong khi đó, một số muối có khả năng khử, như NaHSO3, có thể chuyển đổi các chất có hoá trị cao hơn về hoá trị thấp hơn.
Tóm lại, tính chất hoá học của muối gồm khả năng tan trong nước, khả năng tạo kết tủa, khả năng oxi hóa – khử, và khả năng hấp thụ ánh sáng. Các tính chất này đóng vai trò quan trọng trong các phản ứng và ứng dụng của muối trong cuộc sống hàng ngày.
Cảm ơn bạn đã xem bài viết Tính chất hoá học của muối là gì? Bài tập Hoá lớp 9 tại thcshuynhphuoc-np.edu.vn bạn có thể bình luận, xem thêm các bài viết liên quan ở phía dưới và mong rằng sẽ giúp ích cho bạn những thông tin thú vị.
Từ Khoá Liên Quan:
1. Tính chất hoa học của muối
2. Phản ứng ion của muối
3. Tính chất oxi hóa của muối
4. Tính chất khử của muối
5. Tính chất acid và baz của muối
6. Hoạt tính của muối
7. Phản ứng trao đổi của muối
8. Phản ứng trung hòa muối
9. Tính chất kiềm của muối
10. Tính chất phức tạp của muối
11. Tính chất dẫn điện của muối
12. Tính chất tạo kết tủa của muối
13. Tính chất tạo phản ứng tráng gương của muối
14. Tính chất tạo phản ứng cháy của muối
15. Tính chất tạo phản ứng tan chảy của muối


