Bạn đang xem bài viết NaCl có kết tủa không? Phản ứng hóa học của NaCl và một số chất khác tại thcshuynhphuoc-np.edu.vn bạn có thể truy cập nhanh thông tin cần thiết tại phần mục lục bài viết phía dưới.
Trong lĩnh vực hóa học, nhiều người quan tâm đến khả năng kết tủa của các chất, bao gồm cả muối natri clorua (NaCl). NaCl là một trong những muối phổ biến nhất và thường được sử dụng trong đời sống hàng ngày. Tuy nhiên, khi NaCl tiếp xúc với một số chất khác, liệu có xảy ra hiện tượng kết tủa hay không? Để trả lời cho câu hỏi này, chúng ta cần tìm hiểu về phản ứng hóa học của NaCl và một số chất khác. Bài viết này sẽ giới thiệu tới bạn cơ bản về khả năng kết tủa của NaCl và những phản ứng hóa học mà nó có thể tham gia với một số chất khác.
NaCl Natri Clorua hay còn với cái tên quen thuộc là muối ăn loại gia vị sử dụng hằng ngày với tất cả mọi người. Vậy muối ăn NaCl có kết tủa không, cùng Chúng Tôi tìm hiểu để biết rõ nhất nhé!
NaCl Natri Clorua là chất gì?
Trước khi đi vào đáp án NaCl có kết tủa không. Bây giờ chúng ta sẽ khởi động phần tổng quan về Nacl Natri Clorua nào?
Nguồn gốc của NaCl
Nguồn gốc của NaCl là do một phần xuất phát từ đá trên đáy biển hay ở vùng miệng núi lửa. Tuy nhiên, phần lớn muối NaCl có nguồn gốc ở đất liền.
Từ những giọt nước ngọt sau vài trận mưa không ở dạng tinh khiết 100% mà hòa tan CO2 trong khí quyển rơi xuống đất. Nước mưa này có khoảng 90% các ion Natri hoặc Clo. Hai loại ion này kết hợp với nhau tạo ra muối NaCl.

Cấu trúc của Natri Clorua
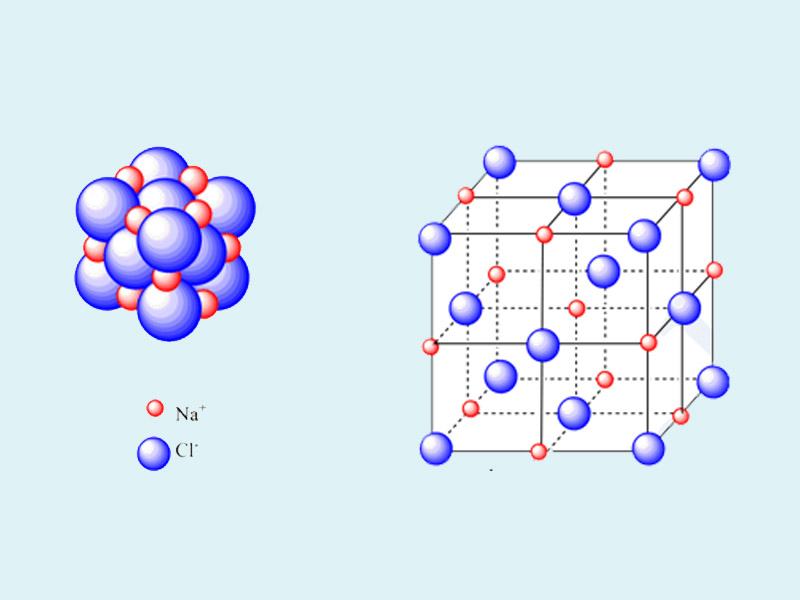
Cấu tạo gồm 1 nguyên tử Na liên kết với 1 nguyên tử Cl bằng liên kết ion.
Có cấu trúc mạng lưới lập phương tâm diện với số phối trí là 6.
Tính chất vật lý và hóa học của NaCl
Tính chất vật lý của NaCl
Các đặc điểm vật lý của muối Natri Clorua là:
- Muối NaCl ở dạng tinh thể, là chất rắn màu trắng hoặc kết tinh không màu và tan tốt trong nước.
- Điểm sôi 1413 độ C, điểm nóng chảy 801 độ C, tỷ trọng 2.16g/cm3.
- Độ hòa tan trong nước 35.9g/ml (25 độ C).
- NaCl tinh khiết không hút ẩm nhưng do bị lẫn tạp chất nên bị chảy rữa khi có không khí.
Tính chất hóa học của NaCl
- NaCl là chất điện li mạnh, phân li hoàn toàn trong nước, tạo ra các ion âm và dương. Ta có: + NaCl → Na+ + Cl-
- Natri Clorua là muối của bazơ khá mạnh và axit mạnh nên nó mang tính trung tính. Vì thế, NaCl tương đối trơ về mặt hóa học.
- PTHH: NaCl + AgNO3 → AgCl↓ + NaNO3
- Tác dụng với nước: Ứng dụng để sản xuất HCl.
Ứng dụng của NaCl
Trong công nghiệp, sản xuất
Trong công nghiệp lượng muối tiêu thụ hàng năm chiếm hơn 80% sản lượng NaCl trên toàn thế giới. Nó tương đương lên đến khoảng 200 triệu tấn.
- Trong công nghiệp sản xuất giày da, người ta sử dụng NaCl để bảo vệ da. Bên cạnh đó, NaCl dùng sản xuất xà phòng, chất tẩy rửa, bột giấy, giấy, thuốc nhuộm, dệt may và sản xuất vải.
- NaCl là nguyên liệu ban đầu để sản xuất chlorine và xút, sử dụng trong hầu hết các ngành công nghiệp.
- Trong sản xuất cao su: NaCl dùng để làm trắng các loại cao su.
- Trong dầu khí: NaCl là thành phần quan trọng trong dung dịch khoan giếng khoan.
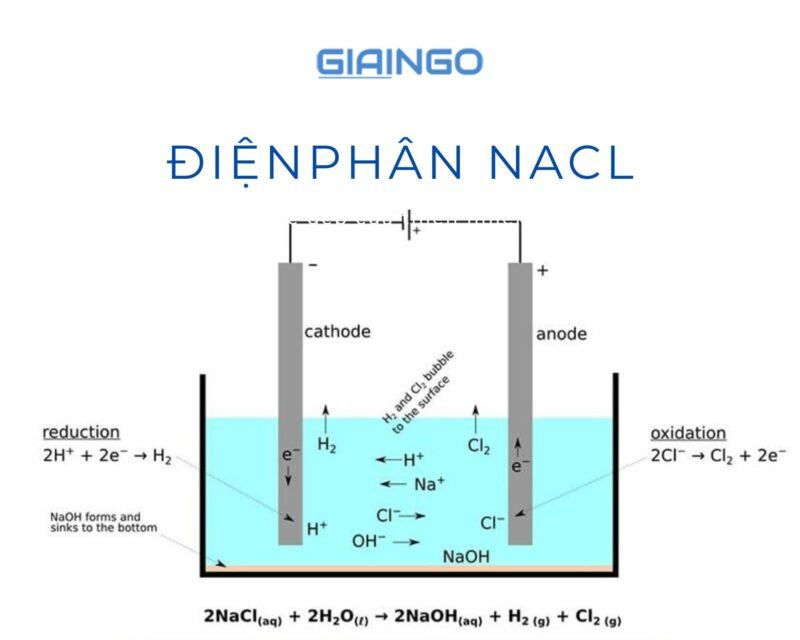
- Từ NaCl có thể chế ra các loại hóa chất dùng cho các ngành khác như điều chế nước Javen, sản xuất nhôm, thép, đồng,… bằng cách điện phân dung dịch hoặc điện phân nóng chảy NaCl có màng ngăn.
Trong nông nghiệp, trồng trọt
- Trong chăn nuôi gia cầm, gia súc: NaCl dùng để cân bằng các quá trình sinh lý trong cơ thể giúp gia súc, gia cầm sẽ tăng trưởng nhanh và giảm bệnh tật.
- Phân loại hạt giống theo trọng lượng.
- Cung cấp thêm yếu tố vi lượng trộn với các loại phân hữu cơ để tăng hiệu quả phân bón.
Trong thực phẩm
NaCl là thành phần chính trong muối ăn và được sử dụng phổ biến trong chế biến thức ăn.
- NaCl dùng muối để ướp thực phẩm sống như hải sản, tôm, cá,… để không bị ươn, hư thối trước khi thực phẩm được nấu.
- NaCl có tính hút ẩm, do đó được sử dụng để bảo quản thực phẩm. Nó làm tăng áp suất thẩm thấu dẫn đến làm cho vi khuẩn bị mất nước và chết.
- NaCl khử mùi thực phẩm, giữ cho trái cây không bị thâm.
- NaCl giúp làm tăng hương vị, kiểm soát quá trình lên men của thực phẩm.

Trong y tế
- NaCl dùng để sát trùng vết thương rất tốt.
- NaCl cung cấp muối khoáng cho cơ thể thiếu nước.
- NaCl có tác dụng thanh lọc cơ thể, khử độc, làm đẹp da, làm trắng răng, chữa viêm họng, chữa hôi miệng,…
- NaCl dùng để pha huyết thanh, trị cảm lạnh, thuốc tiêu độc và một số loại thuốc khác để chữa bệnh cho con người.
Trong đời sống gia đình
- NaCl khử mùi hôi của giày, đuổi kiến.
- NaCl tinh khiết dùng để làm sạch thớt, giữ hoa tươi lâu hơn, làm sạch đồ thủy tinh.
- NaCl giúp lau chảo dính dầu mỡ, chùi sạch tủ lạnh, bàn ủi, tẩy vết rượu vang trên quần áo,…
- NaCl ngâm quần áo trong nước lạnh pha muối giúp quần áo bền màu hơn.
Trong giao thông
Sử dụng muối NaCl tinh khiết để làm tan băng trên đường.

NaCl có kết tủa không?
Khi cho HCl đặc vào dung dịch bão hòa NaCl sẽ tạo thành kết tủa trắng. Khi thêm nước vào hỗn hợp này thì kết tủa sẽ hòa tan lại.
PTHH: 2NaCl + 2HCl → 2NaCl2 + H2
Phản ứng hóa học của NaCl và một số chất khác
K2SO4 NaCl có kết tủa không?
Cho NaCl và K2SO4 tác dụng vs dung dịch BaCl2 thì NaCl ko phản ứng còn K2SO4 thì tạo ra kết tủa trắng đục BaSO4.
PTHH:
BaCl2 + K2SO4 → BaSO4↓(trắng) + 2KCl
BaCl2 + NaCl phương trình không phản ứng.
BaCl2 + NaCl có kết tủa không?
NaCl + BaCl2 không kết tủa, đồng thời không xảy ra phản ứng.
H2SO4 NaCl có kết tủa không?
NaCl H2SO4 có kết tủa trắng.
PTHH:
NaCl + H2SO4 → NaSO4↓(trắng) + 2HCl
Ba(NO3)2 NaCl có kết tủa không?
NaCl Ba(NO3)2 phản ứng không xảy ra, vì thế sẽ không có kết tủa.
NaCl tác dụng với AgNO3 có kết tủa không?
Khi cho dung dịch AgNO3 tác dụng với dung dịch NaCl, sau phản ứng tạo thành bạc clorua không tan có màu trắng.
PTHH: AgNO3 + NaCl → AgCl + NaNO3
Hy vọng qua bài viết của Chúng Tôi sẽ giúp các bạn có được câu trả lời cho câu hỏi NaCl có kết tủa không. Đừng quên theo dõi Chúng Tôi mỗi ngày để tìm hiểu nhiều thông tin thú vị nhé.
Trong kết luận của chủ đề “NaCl có kết tủa không? Phản ứng hóa học của NaCl và một số chất khác”, ta có thể thấy rằng NaCl, hay còn gọi là muối bàn, là một trong những hợp chất phổ biến nhất trong hóa học. NaCl thường tồn tại dưới dạng tinh thể màu trắng, không có kết tủa hoặc hoá học đặc trưng. Đây là một trong những lợi ích lớn của NaCl, khiến nó trở thành một chất được sử dụng rộng rãi trong các ngành công nghiệp và người ta sử dụng nó hàng ngày như một chất ổn định.
Tuy nhiên, trong một số trường hợp, NaCl có thể tạo ra kết tủa khi phản ứng với một số chất khác nhau. Ví dụ, khi NaCl kết hợp với một dung dịch chứa AgNO3 (nitrat bạc), kết tủa AgCl (clorua bạc) sẽ được tạo thành. Kết tủa này xuất hiện dưới dạng một chất rắn màu trắng. Điều này xảy ra do sự tạo thành kết tủa là kết quả của một phản ứng hóa học giữa NaCl và AgNO3, trong đó các ion Cl- từ NaCl tạo kết dính với các ion Ag+ từ AgNO3.
Cũng cần lưu ý rằng, không phải tất cả các chất sẽ tạo kết tủa với NaCl. Ngoài AgCl, một số chất khác như BaCl2 (clorua bari) và Pb(CH3CO2)2 (axetat chì) cũng có khả năng tạo kết tủa khi phản ứng với NaCl. Tuy nhiên, hầu hết các chất khác như MgCl2 (clorua magiê) và Na2SO4 (sunfat natri) không tạo kết tủa khi phối hợp với NaCl.
Tổng kết lại, NaCl tồn tại dưới dạng tinh thể màu trắng, không có kết tủa hoặc hoá học đặc trưng. Tuy nhiên, khi tương tác với một số chất như AgNO3, BaCl2 và Pb(CH3CO2)2, NaCl có khả năng tạo kết tủa. Những hiểu biết này không chỉ cung cấp cho chúng ta một cái nhìn tổng quan về tính chất của NaCl, mà còn giúp ta hiểu rõ thêm về phản ứng hóa học và cách các chất tương tác với nhau.
Cảm ơn bạn đã xem bài viết NaCl có kết tủa không? Phản ứng hóa học của NaCl và một số chất khác tại thcshuynhphuoc-np.edu.vn bạn có thể bình luận, xem thêm các bài viết liên quan ở phía dưới và mong rằng sẽ giúp ích cho bạn những thông tin thú vị.
Từ Khoá Liên Quan:
1. Kết tủa NaCl
2. Tác động của ion trong NaCl
3. Tính tan của NaCl trong nước
4. Phản ứng hóa học NaCl
5. Tạo kết tủa với NaCl
6. Lượng kết tủa của NaCl
7. Tác động của chất lỏng lên NaCl
8. NaCl có kết tủa trong dung dịch axit không?
9. NaCl phản ứng với chất oxi hóa
10. Tương tác giữa NaCl và chất khử
11. NaCl có thể tạo kết tủa với kim loại không?
12. NaCl tan trong dung dịch hoá chất
13. Dung dịch mặn NaCl có phản ứng gì?
14. Tạo kết tủa với NaCl trong điều kiện nào?
15. NaCl có phản ứng với acid sulfat không?


